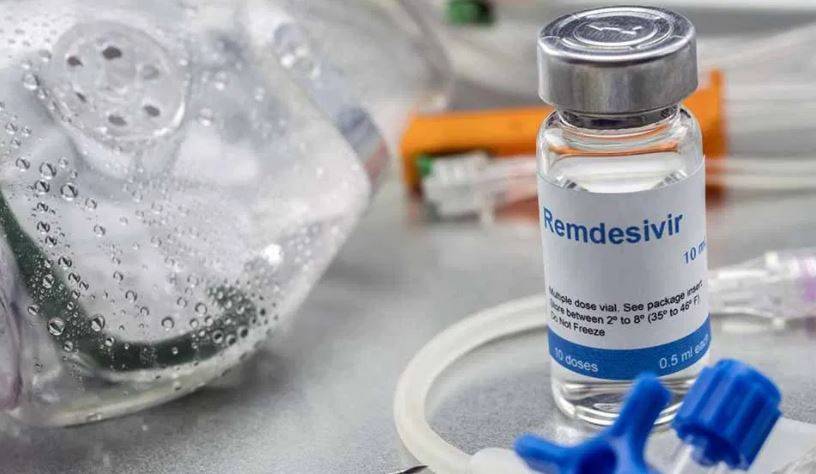
La Cofepris no autorizó el uso del remdesivir como tratamiento para el Covid-19 debido a que las evidencias no sugieres «utilidad suficiente»
Regeneración, 24 de octubre de 2020. El Subsecretario de Prevención y Promoción de la Salud, Hugo López Gatell informó que la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) rechazó la solicitud de autorización sanitaria del remdesivir.
El funcionario señaló que el laboratorio farmacéutico Gilead no ha recibido la autorización sanitaria, pues las evidencias no sugieren “utilidad suficiente” contra el Covid-19.
De acuerdo con expertos en distintos campos de la salud han determinado que la evidencia no sugiere eficacia suficiente en el tratamiento contra la enfermedad.
“La evidencia necesita complementarse con otros elementos de convicción y se le ha solicitado formalmente a Gilead que traiga esta información”, indicó Gatell.
La Agencia de Fármacos y Alimentos (FDA) de Estados Unidos aprobó el uso del remdesivir.
Sin embargo, Gatell comentó que el organismo ha tomado decisiones no convencionales ya que en modalidad de emergencia se reducen los requisitos de evaluación.
“Durante una epidemia, naturalmente, se puede ser un poco menos exigente respecto a la eficacia de un producto porque cualquier beneficio es bienvenido, siempre que la seguridad sea garantizada, esto sí es innegociable”, enfatizó.
Gatell recordó que el remdesivir es un fármaco que se ha investigado mucho pues algunos sugieren que reduce la hospitalización por Covid-19 de tres a cuatros días.
En los resultados preliminares del Ensayo Solidaridad coordinado por la Organización Mundial de la Salud se reveló que no tiene una utilidad significativa en duración de la hospitalización o la mortalidad.