La autorización permitirá el uso de la vacuna a agencias como la Organización Panamericana de la Salud
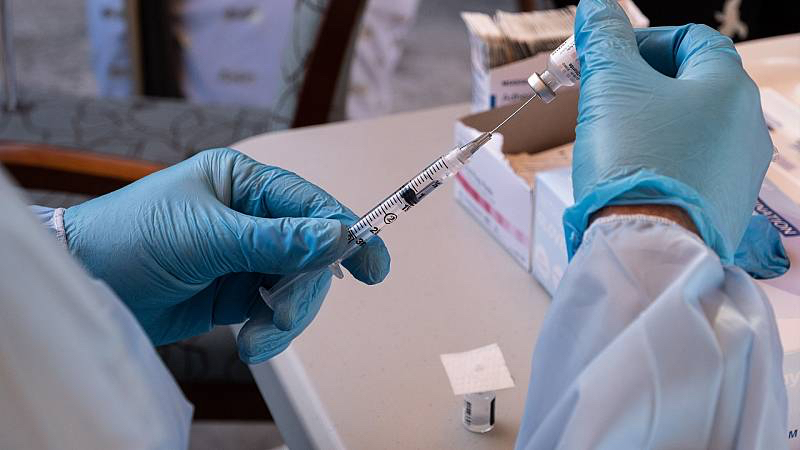
Regeneración, 31 de diciembre de 2020. La OMS anunció su primera autorización para el uso de emergencia de la vacuna contra Covid-19 desarrollada por Pfizer y BioNTech.
Dicha vacuna ya había obtenido la autorización en mercados como Estados Unidos, Reino Unido y la Unión Europea.
Sirve para países que no tienen entidades de homologación de este tipo de productos y abre la puerta a su uso en países de desarrollo.
La autorización permitirá el uso de la vacuna a agencias como la Organización Panamericana de la Salud o el Fondo de las Naciones Unidad para la Infancia (Unicef).
A un año de la pandemia y luego de que expertos del organismo con sede en Ginebra revisarán los datos de seguridad y eficacia de la vacuna Pfizer se logró su autorización.
La OMS admitió que la vacuna presenta desafíos, pues se debe almacenar entre 60 y 90 grados bajo cero.
Ante ello, la OMS trabajará para apoyar a los países en el desarrollo de planes de envío y prepararlos para el uso de la misma.
Por su parte, la doctora Mariangela Simao subrayó que «se necesita un esfuerzo aún mayor para asegurar que se disponga de suficientes dosis de vacunas para satisfacer las necesidades de las poblaciones prioritarias en todo el mundo”.
Cabe señalar que varios millones de personas ya fueron vacunadas con el fármaco, que cuenta con una eficacia del 95%.