Aunque algunos aseguran que el fármaco no ofrece un benefició significativo, la FDA ha autorizado su uso para pacientes con diagnostico de Covid-19.
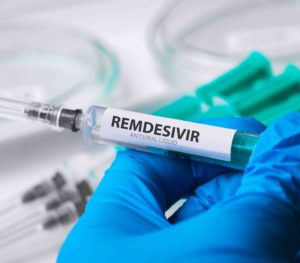
Regeneración, 1 de mayo del 2020. La semana pasada el presidente de Estados Unidos, Donald Trump, informó que la Administración de Drogas y Alimentos de Estados Unidos (FDA, por sus siglas en ingles) había autorizado la utilización de un medicamento experimental para la Covid-19.
La FDA autorizó a Gilead Sciences Inc. Para el uso de emergencia de su medicamento antiviral experimental remdesivir, que serviría para tratar a pacientes diagnosticados con Covid-19.
El presidente ejecutivo de Gilead, Daniel O’Day, calificó la medida como un primer paso importante y dijo que la compañía estaba donando 1 millón de frascos del medicamento para ayudar a los pacientes.
Se informó que el medicamento actuaba mejor cuando se administraba a los pacientes a inicios de la infección. Así lo informó la farmacéutica Gilead.
Gilead ha defendido las perspectivas de remdesivir para ayudar a combatir la pandemia de coronavirus pese a señales de que no ofrece un beneficio significativo.