Cofepris. Producto incumple con las licencias de fabricación y se le atribuye de manera, propiedades terapéuticas, sin embargo, puede causar infección
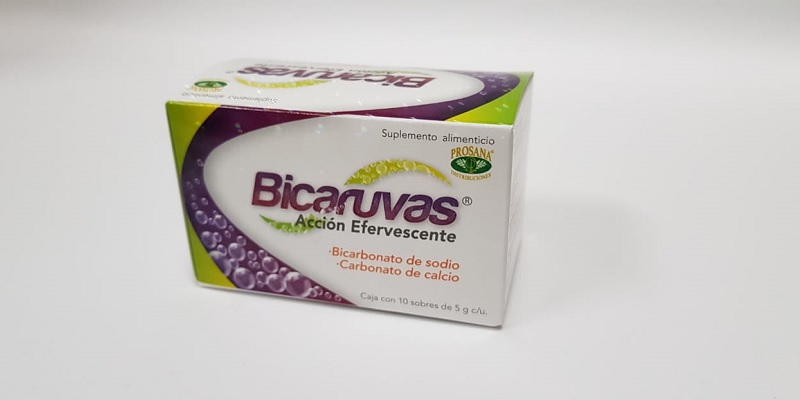
Regeneración, 26 de noviembre del 2019. El producto que se anuncia como auxiliar en las agruras y acidez estomacal, Bicaruvas, presenta malas prácticas de fabricación y puede causar infección, advirtió la Comisión Federal para la Protección contra Riesgos Santitarios (Cofepris).
Faustino Aguilar Arocha, titular de la Cofepris, mencionó que el producto de bicarbonato de sodio y bicarbonato de calcio de la empresa Prosana Distribuciones, incurrió en anomalías infringiendo lo establecido en la Ley General de Salud.
Mencionó que al producto se le atribuye de manera ilegal propiedades terapéuticas.
Además, no cuenta con un registro sanitario, por lo que no se garantiza la calidad y eficacia del producto.
Por esta razón, Aguilar Arocha recomendó a la población no consumir dicho producto que, al igual que otro “producto milagro”, puede causar infección.
Aunque las soluciones abundan, aún no se han aplicado a escala conveniente. El Informe de la Brecha de emisiones da una esperanza a cambio de mayor responsabilidad de los países. https://t.co/ZihpoJh9Rz vía @regeneracionmx
— RegeneraciónMx (@RegeneracionMx) November 27, 2019
________________________________________________________________________
La Cofepris alertó por la impureza de medicamentos con Ranitidina, podrían contener sustancia que incrementa el riego de desarrollar cáncer

Regeneración, 29 de octubre de 2019. La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris), hizo un llamado a la población para que evite el consumo de medicamentos que contengan Ranitidina.
Señaló que quien la tenga prescrita, se le aconseja suspender su ingesta y acudir con el médico para cambiar de tratamiento.
A través de un comunicado, la Cofepris advirtió a los médicos, empresas farmacéuticas suspender la venta y prescripciones de esta medicina.
Esto se debe a que se detectó la impureza N-nitrosodimetilamina (NDMA), una sustancia que incrementa el riesgo de desarrollar cáncer.
Se realizó una investigación y el pasado 5 de octubre se dio a conocer que se comprobó la presencia de N-nitrosodimetilamina en la Ranitidina,por lo que la Cofepris emitió una serie de recomendaciones como medida preventiva.
#Comunicado 📃 La @Cofepris informa sobre los productos que contienen en su formulación el principio activo denominado #Ranitidina 💊 https://t.co/pTqC6bjtVI @SSalud_mx pic.twitter.com/XovvYejLgU
— COFEPRIS (@COFEPRIS) October 6, 2019
La Cofepris emitió las siguientes recomendaciones:
- A la población pidió evitar la compra de medicamentos que contengan Ranitidina y consultar con sus médicos otras opciones terapéuticas.
- En cuanto al personal médico, pidió no prescribir medicamentos que contengan Ranitidina y buscar alternativas terapéuticas.
- A farmacias y distribuidores pidió suspender la comercialización de medicamentos que en su formulación contengan ranitidina.
- A titulares de registros sanitarios de medicamentos que contienen Ranitidina pidió dejar de fabricar, distribuir y vender estos productos.
La Cofepris trabaja para mantener informada a la población y tomar acciones inmediatamente tan pronto los riesgos a la salud sean identificados.
Regeneración, 6 de octubre del 2019. La Cofepris alertó que evalúa riesgos sanitarios en medicamentos que contienen el principio activo ranitidina que se comercializan en México, por posible presencia de la impureza N-nitrosodimetilamina (NDMA), la cual puede incrementar el riesgo de desarrollar cáncer.
La autoridad sanitaria reconoció que por ahora no cuenta con evidencia suficiente para sugerir la suspensión de los tratamientos con ranitidina y en este momento el riesgo de suspenderla es mayor que el de la probable exposición al NDMA.
Agregó que en México se cuenta con otras alternativas de tratamiento autorizadas por la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) para los mismos usos de la ranitidina, por lo que recomendó consultar al médico sobre estas otras opciones.